Conceptos de inmunonutrición aplicados a producción animal
El término inmunonutrición se originó en estudios realizados en la década de 1950, con la sugerencia de que existe una relación entre la desnutrición y las infecciones (Shetty, 2010). A partir de la década de 1970, este concepto comenzó a desglosarse en 4 líneas de cómo la nutrición puede afectar la respuesta inmune:
- La desnutrición (en particular, relacionada con la proteína-energía) y deficiencias de nutrientes;
- La nutrición como factor determinante de la capacidad inmune en recién nacidos y personas de edad avanzada;
- La influencia de la obesidad y la ingesta excesiva de nutrientes en la inmunocompetencia del individuo;
- Y, cómo las interacciones entre la nutrición y la inmunidad repercuten en la medicina clínica y la salud pública (Chandra, 1993).
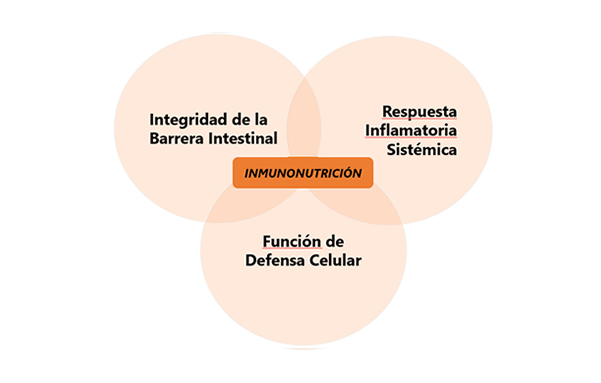
Este concepto se entiende y se aplica a la nutrición animal desde hace mucho tiempo, ya que los conocimientos en las áreas de nutrición, sanidad, manejo y ambiente están bastante avanzados; sin embargo, sólo hace algunos años, el término “inmunonutrición” ha sido efectivamente aplicado. Según McCowen & Bistrian (2003) se clasifican como inmunonutrientes:
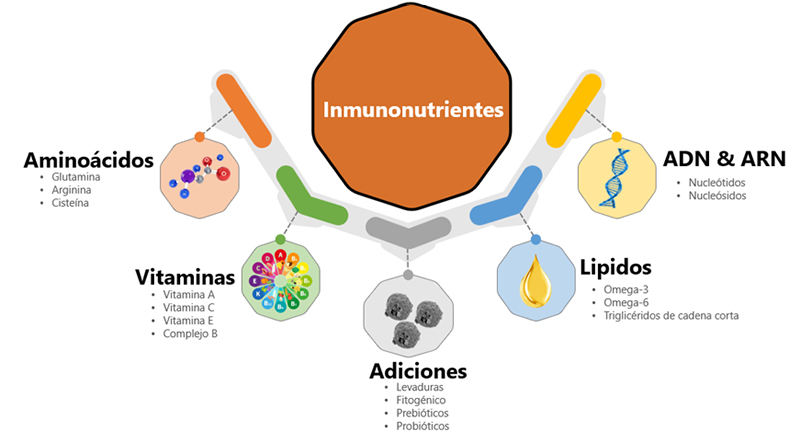
Es importante comprender que el tracto gastrointestinal, además de ser responsable de la digestión y absorción, es también un órgano responsable de las respuestas inmunes. Así pues, su desarrollo y la maduración se ven afectado por factores externos (ambiente, manejo, condiciones sanitarias, dieta, etc.) e inherentes al propio animal (genética, edad). Estos factores también tienen impacto en la microbiota y la salud intestinal. La microbiota intestinal desempeña varias funciones en el organismo y juega un papel importante en la comunicación bidireccional en el eje intestino-cerebro (Cryan & Dinan, 2012). Es decir, el sistema nervioso central (SNC) (a través del eje hipotálamo- hipófisis) puede activarse en respuesta a los factores estresantes y, como resultado, liberar cortisol. El cortisol afectará a las células inmunes, que iniciarán la liberación de citocinas proinflamatorias, que a su vez afectarán la permeabilidad intestinal y lo que permitirá un cambio en la microbiota (Landeiro, 2016).
El epitelio intestinal, además de tener la función de absorber nutrientes, también actúa como barrera física. Si la permeabilidad intestinal se ve afectada, los microorganismos intestinales y los lipopolisacáridos (LPS) pueden pasar a la lámina propia, activando las células del sistema inmunológico y liberando citoquinas proinflamatorias que afectarán el SNC y el sistema entérico (Gareau et al., 2008). Varios cambios metabólicos pueden resultar de estas respuestas, como fiebre, ineficiencias metabólicas, catabolismo del músculo esquelético y síntesis de proteínas de fase aguda (Korver, 2006). Es decir, impactarán en el desvío de nutrientes y energía que se utilizarían para el crecimiento.
De este modo, una respuesta proinflamatoria prolongada generada por cualquiera de estos factores mencionados anteriormente, puede llevar a la deficiencia de la inmunocompetencia del animal. Es de suma importancia que este tenga su capacidad de respuesta y protección construidas a lo largo de su vida, es decir, modulada día a día; ya que el costo metabólico en este caso frente a una respuesta inmune inducida, es bajo e impactará de manera directa en el mantenimiento de la homeostasis metabólica.
El epitelio intestinal, además de tener la función de absorber nutrientes, también actúa como barrera física. Si la permeabilidad intestinal se ve afectada, los microorganismos intestinales y los lipopolisacáridos (LPS) pueden pasar a la lámina propia, activando las células del sistema inmunológico y liberando citoquinas proinflamatorias que afectarán el SNC y el sistema entérico (Gareau et al., 2008). Varios cambios metabólicos pueden resultar de estas respuestas, como fiebre, ineficiencias metabólicas, catabolismo del músculo esquelético y síntesis de proteínas de fase aguda (Korver, 2006). Es decir, impactarán en el desvío de nutrientes y energía que se utilizarían para el crecimiento.
De este modo, una respuesta proinflamatoria prolongada generada por cualquiera de estos factores mencionados anteriormente, puede llevar a la deficiencia de la inmunocompetencia del animal. Es de suma importancia que este tenga su capacidad de respuesta y protección construidas a lo largo de su vida, es decir, modulada día a día; ya que el costo metabólico en este caso frente a una respuesta inmune inducida, es bajo e impactará de manera directa en el mantenimiento de la homeostasis metabólica.
En conclusión, las sustancias que pueden influir en la microbiota, la permeabilidad intestinal y el sistema inmunológico (inmunonutrientes) están interconectadas con la salud, el bienestar y el crecimiento. Aún queda mucho por estudiar sobre el eje microbiota-intestino-cerebro, dada la complejidad de los factores relacionados; sin embargo, el uso de inmunonutrientes, aislados o en combinación trae beneficios comprobados en las diferentes especies. Por tanto, conocer el modo de acción es fundamental para realizar monitoreos correctos, medir los beneficios esperados y cuantificar los retornos a la inversión.
Referencias bibliográficas
Chandra, R. Nutrition and the immune system. Proceedings of the Nutrition Society, 52(1): 77-84, 1993.
Cryan, J. F.; Dinan, T. G. Mind-altering microorganisms: the impact of the gut microbiota on brain and behaviour. Nature Reviews Neuroscience, 13(10): 701–712, 2012.
Gareau, M. G.; Silva, M. A.; Perdue, M. H. Pathophysiological mechanisms of stress-induced intestinal damage. Corrent Molecular Medicine, 8(4): 274–281, 2008.
Korver, D. R. Overview of the Immune Dynamics of the Digestive System. Journal of Applied Poultry Research, 15:123–135, 2006.
Landeiro, J. A. V. R. Impacto da microbiota intestinal na saúde mental. Tese (Doutorado em Ciências Farmacêuticas) – Instituto Superior de Ciências da Saúde Egas Moniz, Almada, Portugal, 81p, 2016.
McCowen K.C; Bistrian B.R. Immunonutrition: problematic or problem solving? The American Journal of Clinical Nutrition, 77(4):764–70, 2003. Shetty, P. Nutrition, immunity e infection. Paperback: 224 pages; Publisher: CABI Publishing; 1 edition 2010
Chandra, R. Nutrition and the immune system. Proceedings of the Nutrition Society, 52(1): 77-84, 1993.
Cryan, J. F.; Dinan, T. G. Mind-altering microorganisms: the impact of the gut microbiota on brain and behaviour. Nature Reviews Neuroscience, 13(10): 701–712, 2012.
Gareau, M. G.; Silva, M. A.; Perdue, M. H. Pathophysiological mechanisms of stress-induced intestinal damage. Corrent Molecular Medicine, 8(4): 274–281, 2008.
Korver, D. R. Overview of the Immune Dynamics of the Digestive System. Journal of Applied Poultry Research, 15:123–135, 2006.
Landeiro, J. A. V. R. Impacto da microbiota intestinal na saúde mental. Tese (Doutorado em Ciências Farmacêuticas) – Instituto Superior de Ciências da Saúde Egas Moniz, Almada, Portugal, 81p, 2016.
McCowen K.C; Bistrian B.R. Immunonutrition: problematic or problem solving? The American Journal of Clinical Nutrition, 77(4):764–70, 2003. Shetty, P. Nutrition, immunity e infection. Paperback: 224 pages; Publisher: CABI Publishing; 1 edition 2010
